Центробежный электроводородный генератор
АЛАМБИК-АЛЬФА
| Исполнители: | |
| Генеральный директор | И. Н. Могилевский |
| Доктор технических наук | Е. М. Кошеляев |
| Доктор технических наук | Е.М. Овсянников |
| Конструктор | В. Е. Чуксин |
| 2004 г. |
Реферат
Показана обоснованность основных положений, положенных в основу разработки принципиально нового способа получения водорода из воды с использованием кинетической и тепловой энергии. Разработана и испытана конструкция электроводородного генератора (ЭВГ). Во время испытаний при использовании сернокислотного электролита на оборотах ротора 1500 об/мин начался электролиз воды и выход водорода (6…8 % объема.) в условиях подсоса воздуха их окружающей среды.
Проведен анализ процесса разложения воды на кислород и водород в процессе воздействия центробежной силы в генераторе. Установлено, что электролиз воды в центробежном генераторе происходит в условиях, существенно отличающихся от существующих в обычных электролизерах:
- увеличении скорости движения и давления по радиусу вращающегося электролита
- активном воздействии на движение ионов электромагнитных полей, наведенных вращающимися зарядами;
- поглощении тепловой энергии из окружающей среды.
Это открывает новые возможности увеличения эффективности электролиза.
Возможность автономного применения ЭВГ не создает проблем хранения и транспорта водорода.
Введение
Попытки за предыдущие 30 лет применить термохимические циклы для разложения воды с использованием более дешевой тепловой энергии по техническим причинам не дали положительного результата.
Технология получения достаточно дешевого водорода из воды с использованием энергии возобновляемых источников и получение при последующей переработке в качестве экологически чистых отходов снова воды (при сжигании в двигателях или при получении электроэнергии в топливных элементах) казались несбыточной мечтой, но с внедрением в практику центробежного электроводородного генератора (ЭВГ) станут реальностью.
ЭВГ предназначен для производства кислород - водородной смеси из воды с использованием кинетической и тепловой энергии. Во вращающийся барабан заливается подогретый электролит, в котором при вращении в результате начинающегося электрохимического процесса происходит разложение воды на водород и кислород.
Модель процесса разложения воды в центробежном поле
Во вращающийся барабан заливается подогретый электролит, в котором при вращении в результате начинающегося электрохимического процесса происходит разложение воды на водород и кислород. ЭВГ разлагает воду с помощью кинетической энергии внешнего источника и тепловой энергии подогретого электролита.
На рис. 1 показана схема движения ионов, молекул воды, электронов, молекул газов водорода и кислорода в ходе электрохимического процесса электролиза воды в кислотном электролите (предполагается, что на распределение молекул в объеме электролита влияет молекулярный вес ионов μ). При добавлении в воду серной кислоты и перемешивании происходит обратимое и равномерное распределение в объеме ионов:
| H2SO4=2H++SO42-, H++H2O=H3O+. | (1) |
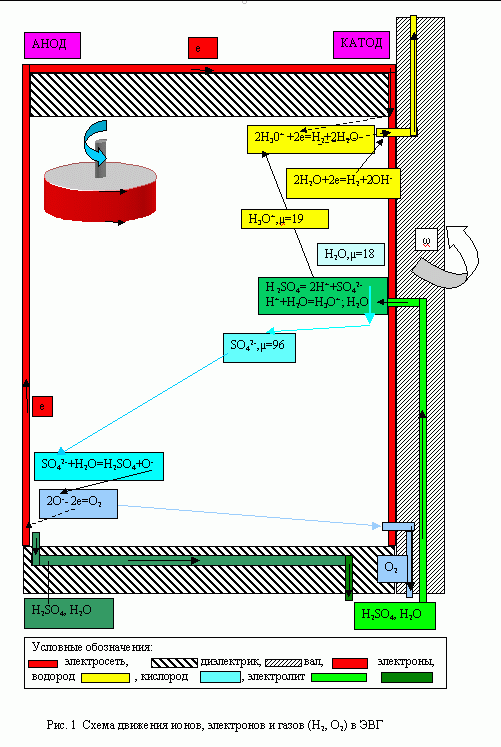
Раствор остается электронейтральным. Ионы и молекулы воды участвуют в броуновском и прочих движениях. С началом вращения ротора под действием центробежной силы происходит расслоение ионов и молекул воды соответственно их массе. Более тяжелые ионы SO42- (μ=96 г/моль) и молекулы воды Н2О (μ=18 г/моль) направляются к ободу ротора. В процессе накопления ионов около обода и образования отрицательного вращающегося заряда формируется магнитное поле. Более легкие положительные ионы Н3О+ (μ=19 г/моль) и молекулы воды (μ=18 г/моль) архимедовыми силами вытесняются в направлении к валу и образуют вращающийся положительный заряд, вокруг которого формируется свое магнитное поле. Известно [1], что магнитное поле оказывает силовое воздействие на находящиеся рядом отрицательные и положительные ионы, не вовлеченные еще в области зарядов вблизи ротора и вала. Анализ силового воздействия магнитного поля, сформированного вокруг этих ионов, показывает, что отрицательно заряженные ионы SO42- магнитной силой прижимаются к ободу, усиливая действие на них центробежной силы, что приводит к активизации их накопления у обода.
Сила воздействия магнитного поля на положительно заряженные ионы H3O+ усиливает действие архимедовой силы, что приводит к активизации их смещения к валу.
Электростатические силы отталкивания одноименных и притяжения разноименных зарядов препятствуют накоплению ионов у обода и вала.
Вблизи вала реакция восстановления водорода начинается при нулевом потенциале платинового катода φ+=0 [8]:
| 2Н3О++2е=Н2+2Н2О, 2Н2О+2е=Н2+2ОН- | (2) |
По мере увеличения числа оборотов вблизи обода накапливаются более тяжелые отрицательные ионы SO42-, и возрастает электрический потенциал φ-, идет реакция:
| SO42-+H2O=H2SO4+O-. | (3) |
Однако восстановление кислорода затягивается до тех пор, пока потенциал анода не достигнет φ-=-1.228 В [8]. После этого электроны иона кислорода получают возможность переходить в платиновый анод (начинается образование молекул кислорода):
| 2О-- 2е=О2. | (4) |
Начинается электролиз, через токовод начинают течь электроны, а через электролит - ионы SO42-.
Образующиеся газы кислород и водород архимедовой силой выдавливаются в область малого давления вблизи вала и затем по каналам, сделанным в вале, выводятся наружу.
Поддержание в замкнутой цепи электрического тока и высокоэффективный ход термохимических реакций (1-4) возможны при обеспечении ряда условий.
Эндотермическая реакция разложения воды требует постоянного подвода тепла в зону реакции.
Из термодинамики электрохимических процессов известно [ 2,3], что для развала молекулы воды необходимо подвести энергию:
| ΔΝо=ΔG+T dS, | (5) |
где тепловая энергия Q=T ΔS (ΔS-изменение энтропии)
ΔG -энергия Гиббса (в обычном электролизере это подведенная электроэнергия).
На сегодня известно, что для разложения воды при нормальных условиях (t=20оС, Р=0.1 МПа) необходимо иметь [2,3]:
| ΔHo=285 кДж/моль, ΔG=237.2 кДж/моль, Q=48.6 кДж/мол | (6) |
Физики признают, что структура воды даже в нормальных условиях, несмотря на длительное изучение, пока не расшифрована [4, 5].
Существующая теоретическая химия имеет серьёзные противоречия с экспериментом, но химики уклоняются от поиска причин этих противоречий, проходят мимо возникающих вопросов. Ответы на них можно получить из результатов анализа структуры молекулы воды. Вот как эта структура представляется на современном этапе её познания (см. рис. 2).
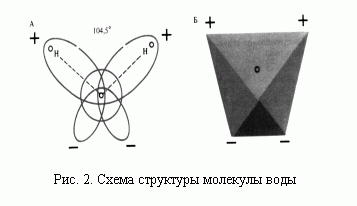
Рис. 2. Схема структуры молекулы воды
Считается, что ядра трех атомов молекулы воды образуют равнобедренный треугольник с двумя протонами, принадлежащими атомам водорода, в основании (рис. 3А), угол между осями Н-О составляет α=104.5о.
Этой информации о структуре молекулы воды недостаточно, чтобы получить ответы на возникшие вопросы и снять выявленные противоречия. Они следуют из анализа энергий химических связей в молекуле воды, поэтому эти энергии должны быть представлены в ее структуре.
Вполне естественно, что в рамках существующих физических и химических представлений о структуре молекулы воды и о процессе её электролиза с целью получения молекулярного водорода, трудно найти ответы на поставленные вопросы, поэтому автор [5] предлагает свои модели структуры молекулы.
Приведенные в [5] результаты расчетов и экспериментов показывают возможность получения дополнительной энергии при электролизе воды, но для этого надо создавать условия для реализации этой возможности.
Необходимо отметить, что электролиз воды в ЭВГ происходит в условиях, существенно отличающихся (и мало изученных) от условий работы промышленных электролизеров. Давление вблизи обода приближается к 2 МПа, окружная скорость обода около 150 м/ с, градиент скорости у вращающейся стенки достаточно велик и вдобавок к этому действуют электростатические и достаточно сильные магнитные поля. В каком направлении при этих условиях изменятся ΔHo, ΔG и Q, пока неизвестно.
Теоретическое описание процесса электромагнитной гидродинамики в электролите ЭВГ также представляет сложную проблему.
На этапе разгона электролита должно быть учтено вязкое взаимодействие ионов и нейтральных молекул воды в условиях воздействия центробежной и вытесняющей более легкие компоненты архимедовой силы, взаимного электростатического отталкивания одноименных ионов при их сближении в процессе образования заряженных областей, магнитного силового воздействия этих областей на движение заряженных ионов к зарядам.
При установившемся движении, когда начался электролиз, во вращающейся среде идет активное радиальное движение ионов (ионный ток) и всплывающих пузырьков образующегося газа, их накопление вблизи вала ротора и отвод наружу, разделение в магнитном поле парамагнитного кислорода и диамагнитного водорода, подвод (отвод) требуемых порций электролита и подключение поступающих ионов к процессу разделения зарядов.
В простейшем случае несжимаемой адиабатически изолированной жидкости при наличии положительных и отрицательно заряженных ионов и нейтральных молекул этот процесс может быть описан (для одной из компонент) в следующем виде [ 9] :
1. Уравнения движения при условии на внешней границе (r=R, V-Vpom):
¶U/¶t=(W× Ñ )U=-grad Ф+D (a × U+b ×W),
¶W/¶t +(U×Ñ)W=-gradФ+D(a× W+b×U),
где V- скорость движения среды, H- напряженность магнитного поля, U=V+H/(4× p × r )0.5, W=V-H/(4× p × r )0.5, Ф=P/r +(U-W)2/8, Р- давление, r - плотность среды, n, n m- кинематическая и “магнитная” вязкость, a =(n+nm)/2, b=(n-n m)/2.
2. Уравнения неразрывности жидкости и замкнутости магнитных силовых линий:
divU=0, divW=0.
3. Уравнение потенциальности электростатического поля:
rotE=0.
4. Уравнения кинетики химических реакций, описывающие процесс превращения веществ (типа (1,3)) может быть описан [2]:
dCa/dτ=v·(Co.a-Ca)/Vе-ra,
где Ca- концентрация продукта химической реакции А (моль/м3),
v-скорость его движения, Vе- объем электролита,
ra-скорость превращения реагентов в продукт химической реакции,
Со.а- концентрация реагентов, подаваемых в зону реакции.
На границе металл- электролит необходим учет кинетики электродных процессов. Некоторые сопутствующие электролизу процессы описаны в электрохимии (электрическая проводимость электролитов, акт химического взаимодействия при соударении химически активных компонент и т.д.) [2], но единых дифференциальных уравнений рассматриваемых процессов пока не существует.
5. Процесс образования газовой фазы в результате электролиза может быть описан с помощью термодинамических уравнений состояния:
yk=f(x1,x2,….xn,T),
где yk- внутренние параметры состояния (давление, температура Т, удельный (мольный) объем), xi- внешние параметры внешних сил, с которыми взаимодействует среда (форма объема электролита, поле центробежных и магнитных сил, условия на границе), но процесс перемещения пузырьков во вращающейся жидкости пока изучен слабо.
Следует отметить, что решения системы приведенных выше дифференциальных уравнений пока получены лишь в немногих простейших случаях.
Эффективность работы ЭВГ может быть получена из баланса энергии путем анализа всех потерь.
При установившемся вращении ротора с достаточным числом оборотов мощность двигателя Nd тратится на:
преодоление аэродинамического сопротивления ротора Na;
потери на трение в подшипниках вала Np;
гидродинамические потери Ngd при разгоне поступающего в ротор электролита, трении его о внутреннюю поверхность деталей ротора, преодолению встречного движения к валу образующихся при электролизе пузырьков газа (см. рис. 1) и т.д.;
поляризационные и омические потери Nom при движении тока в замкнутом контуре в процессе электролиза (см. рис. 1);
подзарядку конденсатора Nk, образованного положительным и отрицательным зарядами;
электролиз Nw.
Оценив величину ожидаемых потерь, можно из баланса энергии определить долю энергии Nwe, расходуемую на разложение воды на кислород и водород:
Nw=Nd –Na-Np-Ngd-Nom-Nk.
Помимо электроэнергии в объем электролита необходимо добавить тепло мощностью Nq=Nwe× Q/DHo (см. выражение (6)).
Тогда полная мощность, расходуемая на электролиз, составит:
Nw=Nwe+Nq.
Эффективность получения водорода в ЭВГ равна отношению полезно полученной энергии водорода Nw к затраченной в двигателе Nd:
h=Nwּк /Nd
где к учитывает неизвестное пока увеличение производительности ЭВГ в условиях воздействия центробежных сил и электромагнитного поля.
Несомненным преимуществом ЭВГ является возможность его автономного использования, когда отпадает необходимость длительного хранения и транспорта водорода.
Результаты испытаний ЭВГ
К настоящему времени проведены успешные испытания двух модификаций ЭВГ, подтвердившие обоснованность разработанной модели процесса электролиза и работоспособности изготовленной модели ЭВГ.
Перед испытаниями была проверена возможность регистрации водорода с помощью газоанализатора АВП-2 [11], датчик которого реагирует только на присутствие водорода в газе. Выделяющийся в ходе активной химической реакции Zn+H2SO4=H2+ZnSO4 водород подавался к АВП-2 с помощью вакуумного компрессора ДС112 по хлорвиниловой трубке диаметром 5 мм и длиной 5м. При начальном уровне фона показаний Vo=0.02 % об. АВП-2 после начала химической реакции объемное содержание водорода увеличилось до V=0.15 % об., что подтвердило возможность обнаружения газа в этих условиях.
При испытаниях 12-18.02.2004 г. в корпус ротора был залит подогретый до 60о С раствор серной кислоты (концентрацией 4 моль/л), нагревший ротор до 40о С. Результаты экспериментальных исследований показали следующее:
1. При вращении электролита (концентрацией 4 моль/л) центробежной силой удалось разделить положительные и отрицательные ионы различного молекулярного веса и образовать заряды в отстоящих друг от друга областях, что привело к возникновению разности потенциалов между этими областями, достаточной для начала электролиза при замыкании тока во внешней электрической цепи.
2. После преодоления электронами потенциального барьера на границе металл- электролит при числе оборотов ротора n=1000…1500 об/мин в начался электролиз воды. При 1500 об/мин анализатором водорода АВП-2 зафиксирован выход водорода V=6…8 % об. в условиях подсоса воздуха из окружающей среды.
3. При снижении оборотов до 500 об/мин электролиз прекращался и показания газоанализатора возвращались к начальным V0=0.02…0.1 % об.; при увеличении оборотов до 1500 об/мин объемное содержание водорода снова возрастало до V=6…8 % об..
При скорости вращения ротора 1500 об/мин обнаружено увеличение выхода водорода в 20 раз при возрастании температуры электролита от t=17о до t=40о С.
Заключение
- Предложена, изготовлена и успешно испытана установка для проверки обоснованности нового предложенного способа разложения воды в поле центробежных сил. При вращении сернокислотного электролита (концентрацией 4 моль/л) в поле центробежных сил произошло разделение положительных и отрицательных ионов различного молекулярного веса и образовались заряды в отстоящих друг от друга областях, что привело к возникновению разности потенциалов между этими областями, достаточной для начала электролиза при замыкании тока во внешней электрической цепи. Начало электролиза зафиксировано при числе оборотов ротора n=1000 об/мин.
При 1500 об/мин водородный газоанализатор АВП-2 показал выделение водорода в объемных процентах 6…8 об.%. - Проведен анализ процесса разложения воды. Показано, что под действием центробежного поля во вращающемся электролите возможно возникновение электромагнитного поля и формирование источника электроэнергии. При определенных оборотах ротора (после преодоления потенциального барьера между электролитом и электродами) начинается электролиз воды. Установлено, что электролиз воды в центробежном генераторе происходит в условиях, существенно отличающихся от существующих в обычных электролизерах:
- увеличении скорости движения и давления по радиусу вращающегося электролита (до 2 МПа);
- активном воздействии на движение ионов электромагнитных полей, наведенных вращающимися зарядами;
- поглощении тепловой энергии из окружающей среды.
Это открывает новые возможности увеличения эффективности электролиза. - В настоящее время ведется разработка следующей более эффективной модели ЭВГ с возможностью измерения параметров вырабатываемого электрического тока, формирующегося магнитного поля, управления током в процессе электролиза, измерением объемного содержания выходящего водорода, его парциального давления, температуры и расхода. Использование этих данных вместе с уже измеряемой электрической мощностью мотора и числом оборотов ротора позволит:
- определить энергетическую эффективность ЭВГ;
- разработать методику расчета основных параметров в условиях промышленного применения;
- наметить пути его дальнейшего совершенствования;
- выяснить пока слабо изученное влияние на электролиз больших давлений, скоростей и электромагнитных полей. - Промышленная установка может быть использована при получении водородного топлива для питания двигателей внутреннего сгорания или иных энергетических и тепловых установок, а также кислорода для технологических нужд в различных отраслях промышленности; получении гремучего газа, например, для газоплазменной технологии в ряде отраслей промышленности и т.д.
- Несомненным преимуществом ЭВГ является возможность автономного использования, когда отпадает необходимость технически сложного длительного хранения и транспорта водорода.
- Технология получения достаточно дешевого водорода из воды с использованием бросовой низкопотенциальной тепловой энергии и выделение при последующем сжигании экологически чистых отходов (снова воды) казались несбыточной мечтой, но с внедрением в практику ЭВГ станут реальностью.
- На изобретение получен ПАТЕНТ № 2224051 от 20.02.2004 г..
- В настоящий момент патентуется покрытие анода и катода, а также электролита, что позволит увеличить производительность электролиза в десятки раз.
Список использованных источников
- Фриш С.Э., Тиморева А.И. Курс общей физики, Том 2, М. –Л., 1952, 616 с.
- Краснов К.С., Воробьев Н.К, Годнев И.Н. и др. Физическая химия. Электрохимия. Химическая кинетика и катализ, М.,“Высшая школа”,2001,219 с.
- Шпильрайн Э.Э., Малышенко С.П., Кулешов Г.Г. Введение в водородную энергетику, 1984,10.
- Путинцев Н.М. Физические свойства льда, пресной и морской воды, Докторская диссертация, Мурманск, 1995,
- Канарев Ф.М. Вода- новый источники энергии, Краснодар, 2000, 155с,
- Зацепин Г.Н. Свойства и структура воды, 1974, 167 с,
- Яворский Б.М., Детлаф А.А. Справочник по физике, М., “Наука”, 1971, 939 с.
- Economics of Non- conventional Hydrogen Production. The Center for Electrochemical Systems and Hydrogen Research, 2002, Engineer, tamh, edutces/ceshr/center.
- Анализатор водорода портативный многофункциональный АВП-2, Фирма “Альфа БАССЕНС”,Кафедра “Биофизика”, МФТИ, М., 2003.